Wat is de anode en kathode - een eenvoudige uitleg
Elektrochemie en galvaniseren
Er zijn twee hoofdsecties in de elektrochemie:
- Galvanische cellen - de productie van elektriciteit door een chemische reactie. Deze elementen omvatten batterijen en accu's. Ze worden vaak chemische stroombronnen genoemd.
- Elektrolyse - de impact op een chemische reactie met elektriciteit, in eenvoudige woorden - met behulp van een stroombron wordt een reactie gestart.
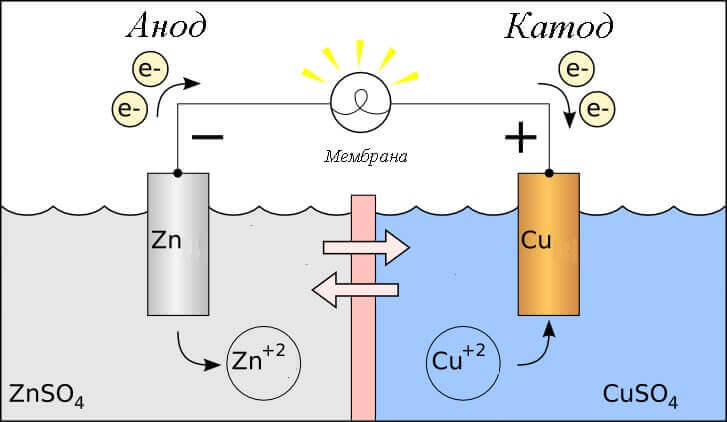
Overweeg de redoxreactie in een galvanische cel, welke processen vinden er dan plaats op de elektroden?
- Anode - de elektrode waarop wordt waargenomen oxidatieve reactiedat wil zeggen, hijgeeft elektronen. De elektrode waarop de oxidatiereactie plaatsvindt, wordt genoemd reductiemiddel.
- Kathode - de elektrode waarop stroomt herstel reactiedat wil zeggen, hijaccepteert elektronen. De elektrode waarop de reductiereactie plaatsvindt, wordt genoemd oxidatiemiddel.
Dit roept de vraag op - waar is het pluspunt en waar is het minpuntje van de batterij? Gebaseerd op de definitie van een galvanische cel anode geeft elektronen.
Belangrijk! GOST 15596-82 geeft een officiële definitie van de namen van de conclusies van chemische stroombronnen, kortom, plus aan de kathode en min aan de anode.
In dit geval wordt rekening gehouden met de stroom van elektrische stroom. langs de geleider van het externe circuit van oxidatiemiddel (kathode) aan reductant (anode). Omdat de elektronen in het circuit van min naar plus stromen en de elektrische stroom omgekeerd, is de kathode een plus en is de anode een min.
Aandacht: stroom vloeit altijd in de anode!
Of hetzelfde in het diagram:
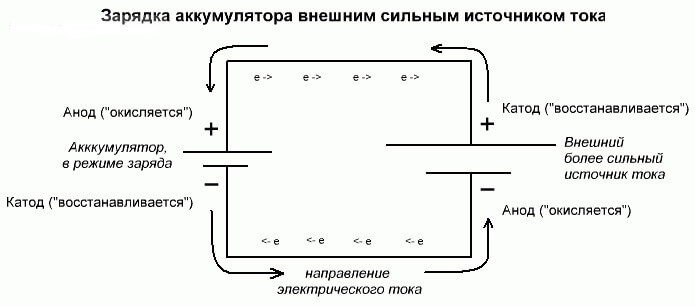
Accu-elektrolyse of laadproces
Deze processen zijn vergelijkbaar en omgekeerd aan de galvanische cel, omdat hier niet de energie afkomstig is van een chemische reactie, maar eerder - er treedt een chemische reactie op vanwege een externe elektriciteitsbron.
In dit geval wordt plus de voeding ook wel de kathode genoemd, en min de anode. Maar de contacten van de oplaadbare galvanische cel of elektroden van de elektrolysator zullen al tegengestelde namen hebben, laten we eens kijken waarom!
Belangrijk! Wanneer een galvanische cel wordt ontladen, is de anode minus, de kathode plus, en omgekeerd tijdens het opladen.
Aangezien de stroom van de positieve pool van de stroombron wordt geleverd aan de positieve pool van de batterij, kan deze laatste geen kathode meer zijn.Onder verwijzing naar het voorgaande kunnen we concluderen dat in dit geval de elektroden van de batterij voorwaardelijk van plaats veranderen tijdens het opladen.
Vervolgens wordt het door de elektrode van een geladen galvanische cel waarin een elektrische stroom stroomt een anode genoemd. Het blijkt dat bij het opladen van de batterij de plus de anode wordt en de min de kathode.
Galvaniseren
De processen van metaalafzetting als gevolg van een chemische reactie onder invloed van een elektrische stroom (tijdens elektrolyse) worden galvanische engineering genoemd. Zo ontving de wereld verzilverde, vergulde, verchroomde of andere met metaal beklede sieraden en details. Dit proces wordt zowel voor decoratieve als voor toegepaste doeleinden gebruikt - om de corrosiebestendigheid van verschillende componenten en assemblages van mechanismen te verbeteren.
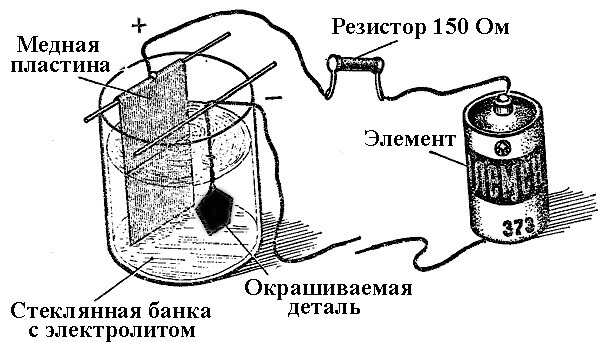
Het werkingsprincipe van galvanische installaties ligt in het gebruik van zoutoplossingen van de elementen die het onderdeel als elektrolyt zullen bedekken.
Bij het galvaniseren is de anode ook een elektrode waarop de positieve uitgang van de stroombron is aangesloten, respectievelijk is de kathode in dit geval een min. In dit geval wordt het metaal afgezet (gereduceerd) op de negatieve elektrode (reductiereactie). Dat wil zeggen, als u met uw eigen handen een vergulde ring wilt maken, sluit u de negatieve uitgang van de voeding erop aan en plaatst u deze in een container met de juiste oplossing.
In de elektronica
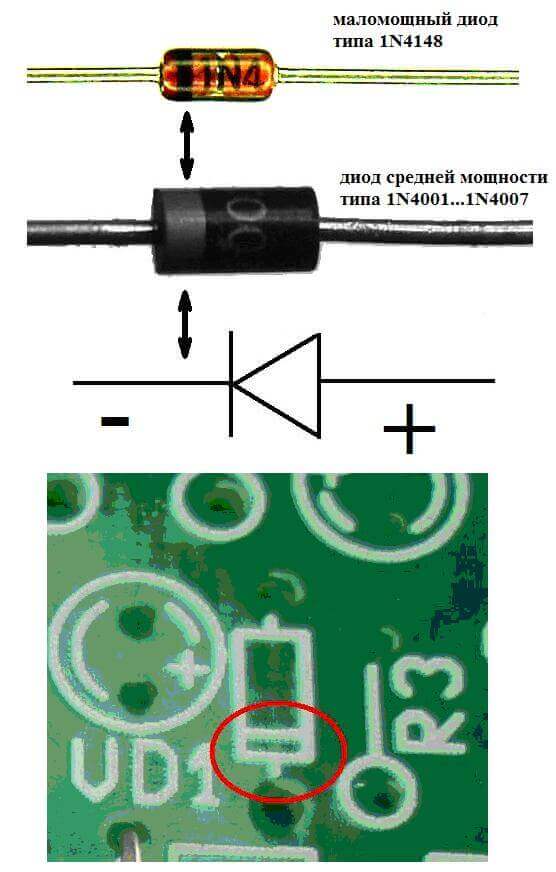
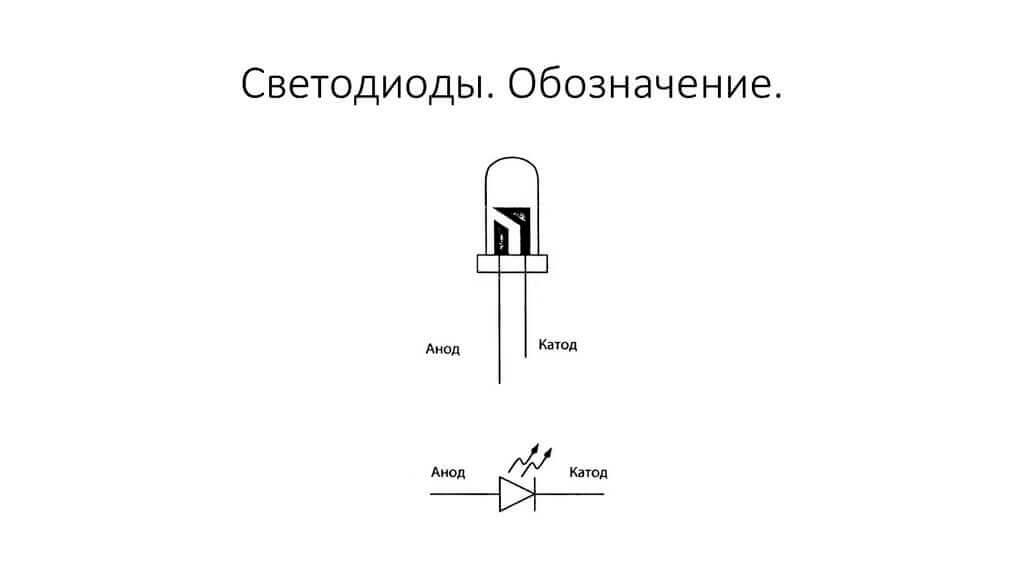
De elektroden of benen van halfgeleider- en vacuüm-elektronische apparaten worden ook vaak de anode en kathode genoemd. Beschouw de voorwaardelijke grafische aanduiding van een halfgeleiderdiode in het diagram:
Zoals we zien, is de anode van de diode verbonden met de plus van de batterij. Het wordt om dezelfde reden zo genoemd - in dit geval stroomt de stroom in ieder geval in de uitgang van de diode. Op een echt element op de kathode zit een markering in de vorm van een strip of een stip.
De LED is vergelijkbaar. Bij 5 mm LED's zijn de binnenkant zichtbaar door de kolf. De helft die groter is, is de kathode.
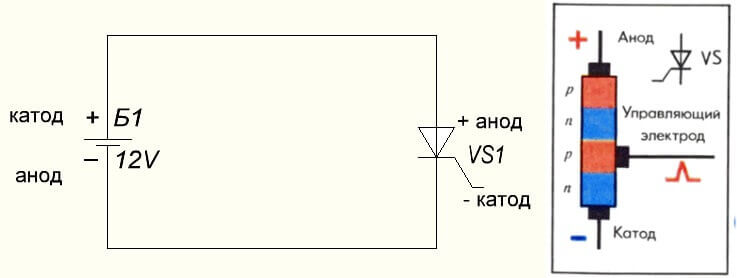
De situatie is ook bij de thyristor, het doel van de conclusies en de "unipolaire" toepassing van deze driepotige componenten maken het een gecontroleerde diode:
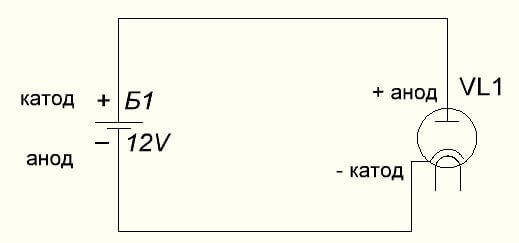
De vacuümdiode verbindt ook de anode met de plus en de kathode met de min, zoals weergegeven in het onderstaande diagram. Hoewel bij het toepassen van sperspanning, de namen van deze elementen niet zullen veranderen, ondanks de stroom van elektrische stroom in de tegenovergestelde richting, zij het onbeduidend.
Bij passieve elementen zoals condensatoren en weerstanden is dit niet het geval. De kathode en de anode zijn niet afzonderlijk van de weerstand geïsoleerd; stroom erin kan in elke richting stromen. U kunt de conclusies een naam geven, afhankelijk van de situatie en de betreffende regeling. Conventionele niet-polaire condensatoren ook. Minder vaak wordt deze scheiding van contactnamen waargenomen in elektrolytische condensatoren.
Conclusie
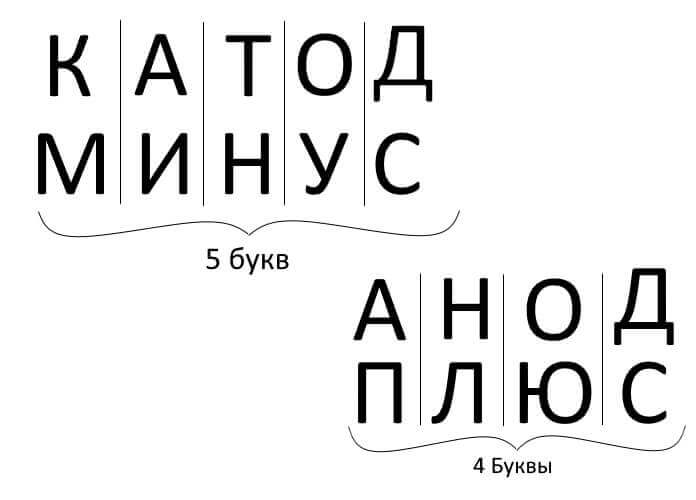
Dus, om samen te vatten, de vraag beantwoorden: hoe te onthouden waar is het pluspunt, waar is de minus van de kathode met de anode? Er is een handige geheugensteun voor elektrolyse, batterijlading, galvanisatie en halfgeleiderapparaten. Deze woorden met vergelijkbare namen hebben hetzelfde aantal letters, zoals hieronder geïllustreerd:
In al deze gevallen stroomt de stroom van de kathode en stroomt in de anode.
Laat u niet verwarren door de verwarring: "waarom is de kathode positief voor de batterij en wordt deze negatief opgeladen als deze wordt opgeladen?" Onthoud voor alle elementen van elektronica, evenals elektrolyzers en bij galvaniseren - in het algemeen is voor alle energieverbruikers de anode de uitgang die is aangesloten op de plus. De verschillen eindigen daar, nu is het gemakkelijker voor u om erachter te komen wat de plus- en minpunten zijn tussen de uitgangen van de elementen en apparaten.
Ten slotte raden we aan om een nuttige video over het onderwerp van het artikel te bekijken:
Nu weet u wat de anode en kathode zijn en hoe u ze snel genoeg kunt onthouden. We hopen dat de verstrekte informatie nuttig en interessant voor je was!
Gerelateerde materialen: